- 5 Sections
- 8 Lessons
- Lifetime
- BAB I DARI SATU SEL KE KERAGAMAN PROSES BIOLOGIS (PERAN NUKLEUS DAN MATERI GENETIK)Bab ini menjadi fondasi konseptual masterclass dengan mengulas bagaimana seluruh keragaman sel dan proses biologis berawal dari satu sel tunggal, yaitu zigot. Pembahasan difokuskan pada peran sentral nukleus dan materi genetik dalam mengatur proliferasi, diferensiasi, serta spesialisasi sel. Mahasiswa diajak memahami bagaimana ekspresi gen, regulasi transkripsi, dan organisasi genom memungkinkan munculnya ratusan tipe sel dengan fungsi yang berbeda meskipun membawa informasi genetik yang sama. Bab ini menanamkan perspektif bahwa kompleksitas kehidupan bersumber dari regulasi, bukan sekadar keberadaan gen.2
- BAB II PROTEIN STAT3 SEBAGAI PENGAMBIL KEPUTUSAN MOLEKULER DALAM SEBUAH SELBab ini membahas STAT3 sebagai contoh konkret protein regulator yang berperan sebagai “decision maker” molekuler di dalam sel. STAT3 dipelajari tidak hanya sebagai faktor transkripsi, tetapi sebagai simpul integrasi berbagai sinyal ekstraseluler dan intraseluler. Pembahasan mencakup aktivasi STAT3, regulasi domain strukturalnya, serta implikasinya terhadap nasib sel, seperti proliferasi, diferensiasi, survival, dan respons stres. Bab ini menekankan bagaimana satu protein dapat menentukan arah perilaku sel melalui jaringan regulasi yang kompleks.4
- 2.12.1. Struktur dan Fungsi Protein STAT3 (Domain Protein, Target Inhibitor, dan Relevansinya pada Kondisi Normal dan Penyakit Osteoporosis)45 Minutes
- 2.2Kuis 2.14 Questions
- 2.32.2. Regulasi Aktivitas STAT3 oleh Jalur Persinyalan Hulu (Fokus JAK1/2–STAT3 Signaling, Senyawa Inhibitor JAK1/2, dan Implikasinya pada Rheumatoid Arthritis; RA)45 Minutes
- 2.4Kuis 2.24 Questions
- BAB III PENUAAN SEBAGAI PROSES BIOLOGIS YANG TERKONTROL DAN MENGARAH PADA DISREGULASIBab ini menggeser sudut pandang penuaan dari sekadar proses pasif akibat akumulasi kerusakan menjadi proses biologis yang relatif terprogram dan dikendalikan. Mahasiswa diajak memahami penuaan sebagai hasil perubahan bertahap dalam regulasi molekuler, jaringan sinyal, dan homeostasis seluler. Bab ini juga mengkaji bagaimana kegagalan mekanisme regulasi tersebut berujung pada kondisi disregulasi yang meningkatkan kerentanan terhadap penyakit degeneratif. Dengan demikian, penuaan diposisikan sebagai fenomena biologis yang dapat dipelajari, dimodelkan, dan berpotensi dimodulasi.4
- BAB IV INTERVENSI TERAPEUTIK MOLEKULER BERBASIS REGULASI SISTEMATIKBab ini membahas pendekatan terapeutik modern yang tidak lagi berfokus pada satu target tunggal, melainkan pada regulasi sistem biologis secara menyeluruh. Mahasiswa diperkenalkan pada konsep intervensi molekuler yang menargetkan jalur sinyal, jaringan regulasi gen, dan keseimbangan sistemik sel. Bab ini mengintegrasikan pengetahuan tentang STAT3, penuaan, dan regulasi sel untuk memahami bagaimana terapi dapat dirancang secara rasional, adaptif, dan kontekstual terhadap kompleksitas sistem biologis.4
- BAB V UJIAN AKHIR MASTERCLASS OSN #0001Bab ini merupakan tahap evaluasi akhir yang dirancang untuk mengukur pemahaman konseptual, kemampuan analisis, dan integrasi pengetahuan peserta terhadap seluruh materi masterclass. Ujian tidak hanya menilai penguasaan fakta, tetapi juga kemampuan berpikir tingkat tinggi, seperti penalaran biologis, interpretasi fenomena molekuler, dan penerapan konsep dalam konteks baru. Bab ini menegaskan tujuan utama masterclass, yaitu membentuk cara berpikir biologis yang sistemik, kritis, dan kompetitif sesuai standar OSN Biologi.3
Curriculum
4.2. Metformin sebagai Intervensi Terapeutik Hibrid (Inhibitor dan Aktivator Tidak Langsung dalam Regulasi Metabolisme Sel)
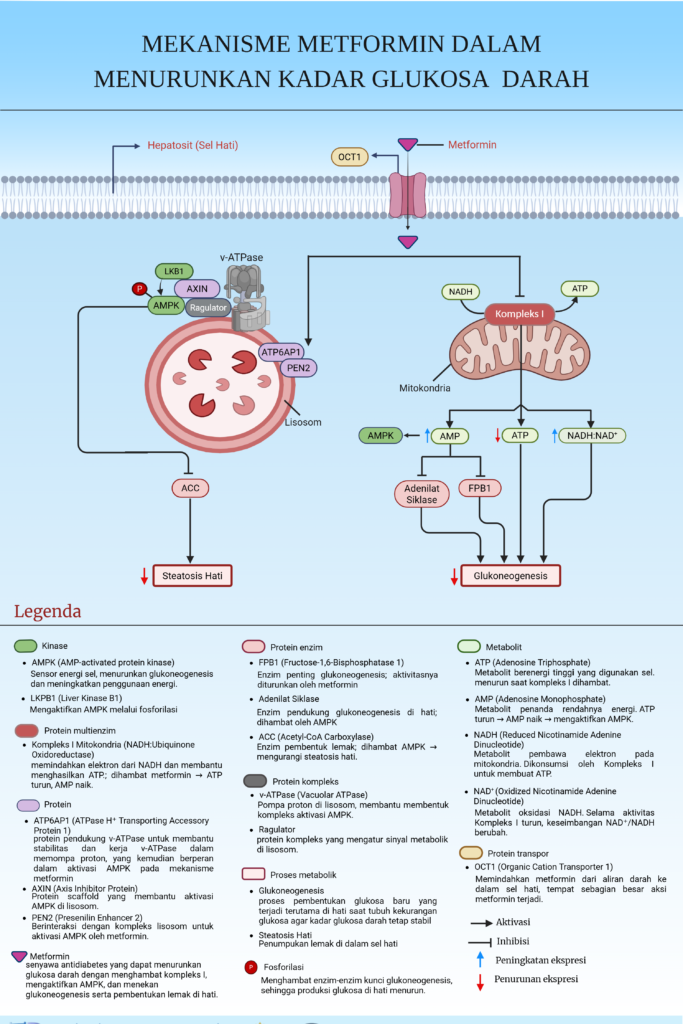
Salah satu lokasi kunci aksi metformin adalah sel hati (hepatosit), karena hati merupakan organ utama pengatur produksi glukosa endogen melalui proses glukoneogenesis. Pada kondisi diabetes melitus tipe 2, hepatosit sering berada dalam keadaan overproduksi glukosa, meskipun kadar glukosa darah sudah tinggi. Kondisi ini mencerminkan kegagalan regulasi metabolik, di mana hati terus “mengirim glukosa” ke sirkulasi tanpa memperhatikan status energi sistemik.
Ilustrasi menunjukkan bahwa metformin memasuki hepatosit melalui transporter OCT1, lalu memicu dua mekanisme utama yang saling terhubung: penghambatan glukoneogenesis dan penurunan steatosis hati. Kedua proses ini tidak hanya bergantung pada mitokondria, tetapi juga melibatkan lisosom sebagai pusat integrasi sinyal metabolik.
Pada tingkat glukoneogenesis, metformin menurunkan produksi glukosa hati melalui kombinasi perubahan status energi sel dan inhibisi enzim kunci glukoneogenik. Penghambatan Kompleks I mitokondria menurunkan produksi ATP dan meningkatkan rasio AMP/ATP. Perubahan ini mengaktifkan AMPK, yang kemudian menekan aktivitas enzim glukoneogenesis seperti fructose-1,6-bisphosphatase (FBP1) serta menurunkan dukungan sinyal dari adenilat siklase. Akibatnya, jalur pembentukan glukosa baru dari substrat non-karbohidrat menjadi tidak efisien, sehingga output glukosa dari hepatosit menurun.
Namun, ilustrasi juga menyoroti mekanisme yang lebih baru dan penting, yaitu aktivasi AMPK yang dimediasi lisosom. Metformin memicu perakitan kompleks sinyal di membran lisosom yang melibatkan v-ATPase, AXIN, LKB1, ATP6AP1, dan PEN2. Kompleks ini bertindak sebagai platform sensing metabolik, yang memungkinkan AMPK diaktifkan tanpa harus sepenuhnya bergantung pada perubahan AMP sitosolik. Mekanisme ini menjelaskan mengapa metformin tetap efektif menekan glukoneogenesis bahkan pada kondisi tertentu ketika perubahan energi mitokondria tidak dominan.
Selain menekan produksi glukosa, aktivasi AMPK di hepatosit juga berdampak langsung pada steatosis hati, yaitu penumpukan lemak berlebih di sel hati yang sering menyertai diabetes tipe 2 dan resistensi insulin. AMPK menghambat aktivitas acetyl-CoA carboxylase (ACC), enzim kunci dalam sintesis asam lemak. Inhibisi ACC menurunkan pembentukan lipid baru dan mendorong penggunaan asam lemak sebagai sumber energi. Dengan demikian, metformin membantu mengurangi akumulasi lemak di hepatosit, memperbaiki fungsi hati, dan menurunkan stres metabolik kronis.
Dengan menghubungkan lisosom, AMPK, glukoneogenesis, dan steatosis hati, ilustrasi ini menegaskan bahwa metformin tidak bekerja sebagai “obat penurun gula” yang sederhana. Sebaliknya, metformin bertindak sebagai pengatur ulang keputusan metabolik hepatosit, mengalihkan sel hati dari mode produksi glukosa dan penyimpanan lemak menuju mode efisiensi energi dan homeostasis. Perspektif ini memperkuat pemahaman bahwa diabetes tipe 2 adalah penyakit disregulasi metabolik seluler, dan bahwa intervensi efektif harus menarget pusat pengambilan keputusan metabolik, bukan hanya gejala akhirnya berupa hiperglikemia.