- 5 Sections
- 8 Lessons
- Lifetime
- BAB I DARI SATU SEL KE KERAGAMAN PROSES BIOLOGIS (PERAN NUKLEUS DAN MATERI GENETIK)Bab ini menjadi fondasi konseptual masterclass dengan mengulas bagaimana seluruh keragaman sel dan proses biologis berawal dari satu sel tunggal, yaitu zigot. Pembahasan difokuskan pada peran sentral nukleus dan materi genetik dalam mengatur proliferasi, diferensiasi, serta spesialisasi sel. Mahasiswa diajak memahami bagaimana ekspresi gen, regulasi transkripsi, dan organisasi genom memungkinkan munculnya ratusan tipe sel dengan fungsi yang berbeda meskipun membawa informasi genetik yang sama. Bab ini menanamkan perspektif bahwa kompleksitas kehidupan bersumber dari regulasi, bukan sekadar keberadaan gen.2
- BAB II PROTEIN STAT3 SEBAGAI PENGAMBIL KEPUTUSAN MOLEKULER DALAM SEBUAH SELBab ini membahas STAT3 sebagai contoh konkret protein regulator yang berperan sebagai “decision maker” molekuler di dalam sel. STAT3 dipelajari tidak hanya sebagai faktor transkripsi, tetapi sebagai simpul integrasi berbagai sinyal ekstraseluler dan intraseluler. Pembahasan mencakup aktivasi STAT3, regulasi domain strukturalnya, serta implikasinya terhadap nasib sel, seperti proliferasi, diferensiasi, survival, dan respons stres. Bab ini menekankan bagaimana satu protein dapat menentukan arah perilaku sel melalui jaringan regulasi yang kompleks.4
- 2.12.1. Struktur dan Fungsi Protein STAT3 (Domain Protein, Target Inhibitor, dan Relevansinya pada Kondisi Normal dan Penyakit Osteoporosis)45 Minutes
- 2.2Kuis 2.14 Questions
- 2.32.2. Regulasi Aktivitas STAT3 oleh Jalur Persinyalan Hulu (Fokus JAK1/2–STAT3 Signaling, Senyawa Inhibitor JAK1/2, dan Implikasinya pada Rheumatoid Arthritis; RA)45 Minutes
- 2.4Kuis 2.24 Questions
- BAB III PENUAAN SEBAGAI PROSES BIOLOGIS YANG TERKONTROL DAN MENGARAH PADA DISREGULASIBab ini menggeser sudut pandang penuaan dari sekadar proses pasif akibat akumulasi kerusakan menjadi proses biologis yang relatif terprogram dan dikendalikan. Mahasiswa diajak memahami penuaan sebagai hasil perubahan bertahap dalam regulasi molekuler, jaringan sinyal, dan homeostasis seluler. Bab ini juga mengkaji bagaimana kegagalan mekanisme regulasi tersebut berujung pada kondisi disregulasi yang meningkatkan kerentanan terhadap penyakit degeneratif. Dengan demikian, penuaan diposisikan sebagai fenomena biologis yang dapat dipelajari, dimodelkan, dan berpotensi dimodulasi.4
- BAB IV INTERVENSI TERAPEUTIK MOLEKULER BERBASIS REGULASI SISTEMATIKBab ini membahas pendekatan terapeutik modern yang tidak lagi berfokus pada satu target tunggal, melainkan pada regulasi sistem biologis secara menyeluruh. Mahasiswa diperkenalkan pada konsep intervensi molekuler yang menargetkan jalur sinyal, jaringan regulasi gen, dan keseimbangan sistemik sel. Bab ini mengintegrasikan pengetahuan tentang STAT3, penuaan, dan regulasi sel untuk memahami bagaimana terapi dapat dirancang secara rasional, adaptif, dan kontekstual terhadap kompleksitas sistem biologis.4
- BAB V UJIAN AKHIR MASTERCLASS OSN #0001Bab ini merupakan tahap evaluasi akhir yang dirancang untuk mengukur pemahaman konseptual, kemampuan analisis, dan integrasi pengetahuan peserta terhadap seluruh materi masterclass. Ujian tidak hanya menilai penguasaan fakta, tetapi juga kemampuan berpikir tingkat tinggi, seperti penalaran biologis, interpretasi fenomena molekuler, dan penerapan konsep dalam konteks baru. Bab ini menegaskan tujuan utama masterclass, yaitu membentuk cara berpikir biologis yang sistemik, kritis, dan kompetitif sesuai standar OSN Biologi.3
Curriculum
2.2. Regulasi Aktivitas STAT3 oleh Jalur Persinyalan Hulu (Fokus JAK1/2–STAT3 Signaling, Senyawa Inhibitor JAK1/2, dan Implikasinya pada Rheumatoid Arthritis; RA)
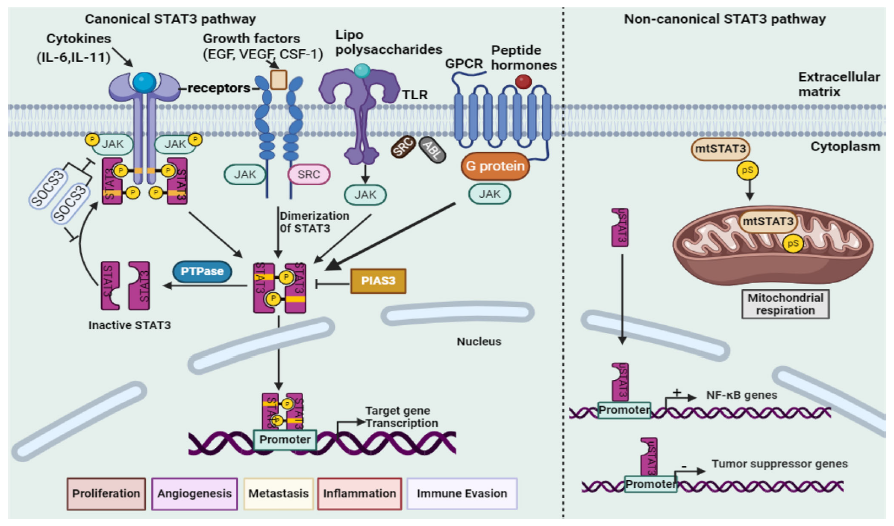
Jika di pelajaran sebelumnya (2.1) STAT3 kita ibaratkan sebagai pengambil keputusan molekuler, maka beberapa Gambar 1 dari Samad et al. (2025) berikut ini menunjukkan bahwa protein STAT3 ini bekerja seperti pusat komando, yang menerima berbagai sinyal dari luar sel dan menerjemahkannya menjadi keputusan biologis di dalam sel. Keputusan tersebut bisa berupa peradangan (inflamasi), pertumbuhan sel, diferensiasi, hingga kematian sel. Karena itulah, ketika STAT3 terlalu aktif atau terlalu lama menyala (on), dampaknya dapat dirasakan di banyak sistem tubuh secara sekaligus.
Pada jalur STAT3 yang bersifat kanonik (jalur klasik), prosesnya dimulai dari sinyal yang sangat familiar dalam biologi penyakit, yaitu sitokin. Sitokin seperti IL-6 dan IL-11 berikatan dengan reseptornya di membran sel, yang melibatkan protein gp130. Ikatan ini mengaktifkan enzim JAK1 dan JAK2, yang kemudian memfosforilasi STAT3. Setelah mengalami fosforilasi, STAT3 berpasangan (berdimer), berpindah ke nukleus, lalu mengaktifkan gen-gen target. Gambar 1 (jalur STAT3 kanonikal) memperlihatkan bahwa gen-gen target STAT3 bukan gen sembarangan. Gen-gen ini mengatur proses yang sangat fundamental, seperti proliferasi sel, pembentukan pembuluh darah (angiogenesis), peradangan, metastasis, hingga penghindaran sistem imun. Tidak mengherankan jika aktivasi STAT3 yang berlebihan sering ditemukan pada kanker, penyakit autoimun, dan peradangan kronis.
Menariknya, tubuh sebenarnya memiliki sistem rem untuk mencegah STAT3 bekerja terlalu jauh. Protein seperti SOCS3, PIAS3, dan fosfatase bertugas menurunkan atau mematikan sinyal STAT3 setelah tugasnya selesai. Dalam kondisi sehat, sistem ini memastikan bahwa STAT3 hanya aktif sementara dan terkontrol. Masalah muncul ketika sistem rem ini gagal, sehingga STAT3 terus aktif tanpa henti.
Namun, cerita STAT3 tidak berhenti di nukleus. Ilustrasi kedua (Gambar 1) dari Samad et al. juga memperkenalkan jalur STAT3 non-kanonik, yang mungkin terdengar asing bagi banyak peserta. Pada jalur ini, STAT3 tidak bekerja sebagai faktor transkripsi, melainkan masuk ke mitokondria. Di mitokondria, STAT3, yang dikenal sebagai mtSTAT3, berperan dalam mengatur respirasi mitokondria, metabolisme energi, dan keseimbangan oksidatif sel.
Dengan kata lain, STAT3 tidak hanya mengatur apa yang ditulis gen, tetapi juga bagaimana sel menghasilkan energi. Inilah sebabnya mengapa STAT3 sering dikaitkan dengan sel kanker yang metaboliknya sangat aktif, serta dengan sel inflamasi yang membutuhkan energi besar untuk mempertahankan peradangan kronis. Jalur non-kanonik ini menjelaskan mengapa menghambat STAT3 kadang memberi efek luas, bahkan di luar regulasi gen.
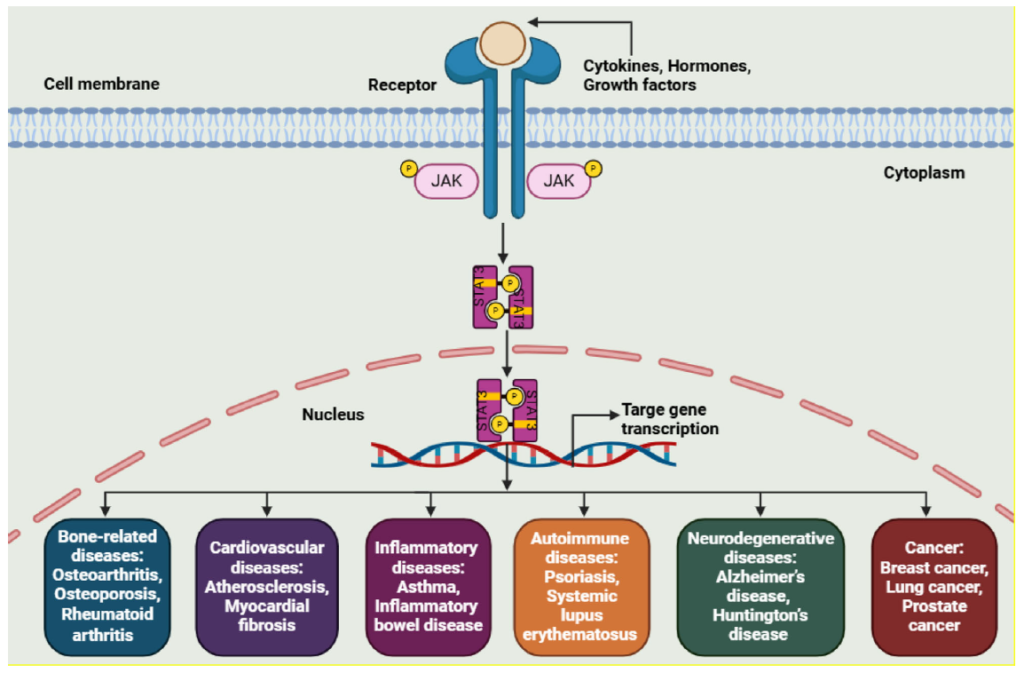
Ilustrasi ketiga memperluas perspektif kita lebih jauh: aktivasi STAT3 berbasis reseptor ternyata terlibat dalam berbagai penyakit lintas sistem. Di jaringan tulang, STAT3 berperan pada osteoporosis, osteoartritis, dan rheumatoid arthritis. Di sistem kardiovaskular, ia terlibat dalam aterosklerosis dan fibrosis jantung. Pada sistem imun dan inflamasi, STAT3 berkontribusi terhadap asma, inflammatory bowel disease, psoriasis, dan lupus. Bahkan pada sistem saraf, STAT3 dikaitkan dengan penyakit Alzheimer dan Huntington. Daftar ini menegaskan satu hal penting: STAT3 adalah regulator multisistem, bukan protein spesifik satu penyakit.
Karena posisinya yang sangat sentral, STAT3 menjadi target terapi yang sangat menarik. Ilustrasi “therapeutic targeting of STAT3” menunjukkan bahwa jalur ini dapat diserang dari berbagai arah. Kita bisa menarget sitokin atau reseptornya menggunakan antibodi monoklonal, menekan sinyal hulu dengan JAK inhibitors, atau langsung menghambat STAT3 melalui inhibitor domain SH2, inhibitor pengikatan DNA, hingga pendekatan modern seperti antisense oligonucleotide (ASO) dan protein degrader (PROTAC).
Pendekatan yang beragam ini mencerminkan satu kesadaran penting dalam biologi modern: STAT3 tidak bisa diperlakukan sebagai saklar on-off sederhana. Terlalu banyak fungsi penting yang bergantung padanya. Karena itu, strategi terapi masa depan bukan lagi “mematikan STAT3”, melainkan mengatur kapan, di mana, dan bagaimana STAT3 bekerja.
Dari sudut pandang pembelajaran, rangkaian ilustrasi (gambar 1-4) ini membantu kita memahami benang merah antara sinyal di membran sel, keputusan molekuler di nukleus dan mitokondria, serta manifestasi klinis penyakit. STAT3 menjadi contoh ideal bahwa satu protein, jika ditempatkan di simpul yang tepat dalam jaringan sinyal, mampu menjelaskan mengapa penyakit yang tampak berbeda, dari osteoporosis hingga kanker, dapat memiliki akar molekuler yang sama.
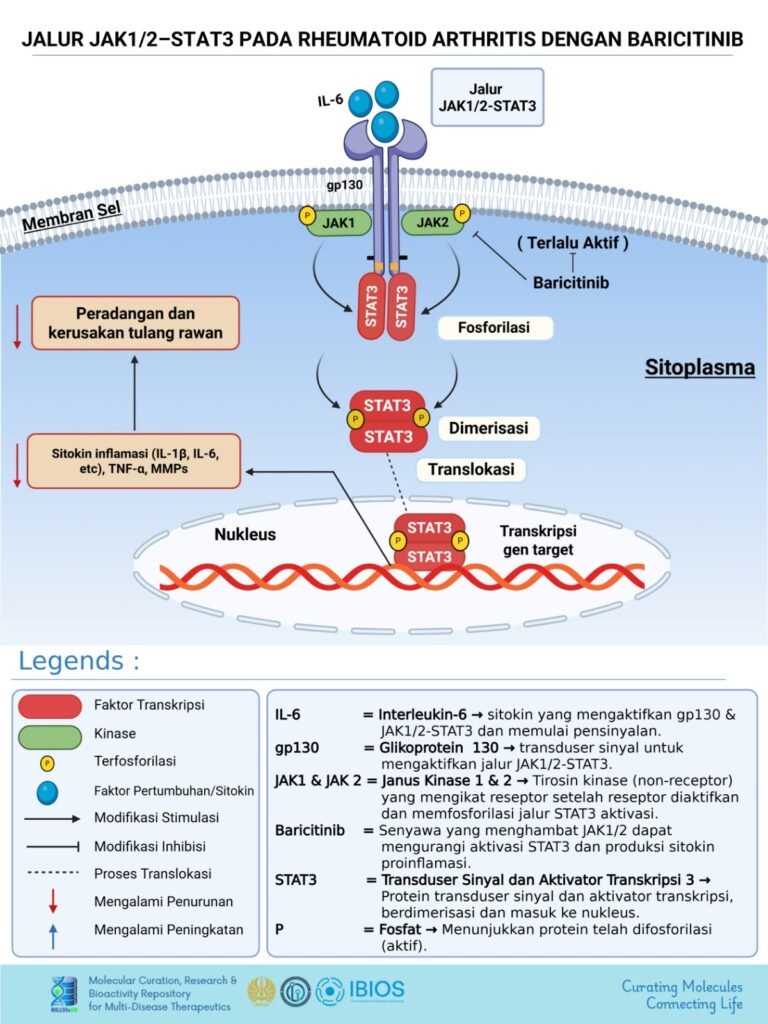
Strategi untuk meregulasi STAT3 tidak harus selalu dicapai dengan menghambat STAT3 secara langsung. Sebaliknya, jalur persinyalan STAT3 menyediakan banyak titik intervensi terapeutik, mulai dari hulu hingga hilir, yang masing-masing memiliki konsekuensi biologis dan klinis yang berbeda. Dengan kata lain, STAT3 dapat dikendalikan melalui beragam strategi, tergantung pada konteks penyakit dan tujuan terapi.
Pada bagian paling hulu, ilustrasi menunjukkan bahwa sinyal STAT3 dapat ditekan dengan antibodi monoklonal yang menarget sitokin atau reseptornya, seperti IL-6 atau IL-6R (misalnya siltuximab, tocilizumab, atau sarilumab). Pendekatan ini bekerja dengan mencegah sinyal inflamasi sejak awal, sebelum mencapai mesin transduksi sinyal intraseluler. Strategi ini banyak digunakan pada penyakit inflamasi dan autoimun, termasuk rheumatoid arthritis.
Sedikit lebih ke hilir, jalur STAT3 dapat diregulasi melalui inhibitor JAK, seperti tofacitinib, ruxolitinib, atau baricitinib (Gambar 3). Obat-obatan ini tidak menarget STAT3 secara langsung, tetapi memutus aliran sinyal hulu yang diperlukan untuk fosforilasi dan aktivasi STAT3. Pendekatan ini bersifat lebih luas, karena satu inhibitor JAK dapat memengaruhi beberapa jalur sitokin sekaligus.
Ilustrasi juga memperlihatkan strategi yang lebih spesifik dan bertarget, yaitu STAT3 inhibitors langsung, terutama yang menarget domain SH2. Senyawa seperti Stattic atau inhibitor lain pada kelas ini bekerja dengan menghambat dimerisasi STAT3, sehingga STAT3 gagal masuk ke nukleus dan mengaktifkan gen target. Pendekatan ini menarik karena lebih selektif terhadap STAT3 sebagai faktor transkripsi.
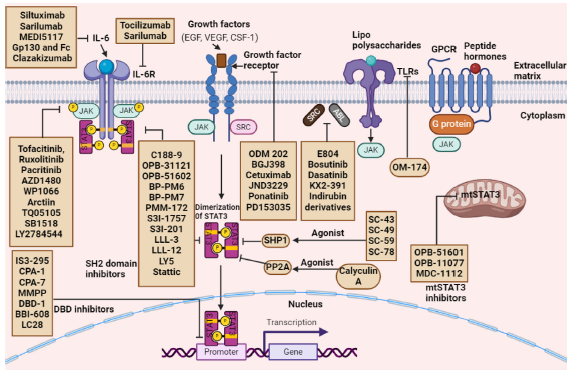
Selain itu, terdapat pula pendekatan yang menarget fungsi transkripsi STAT3 melalui domain pengikat DNA (DBD), misalnya dengan oligonukleotida decoy, yang “menipu” STAT3 agar berikatan pada DNA umpan, bukan pada promotor gen target. Strategi ini menunjukkan bahwa bahkan setelah STAT3 aktif dan berada di nukleus, aktivitasnya masih dapat dikendalikan.
Yang lebih menarik lagi, ilustrasi ini juga menampilkan jalur STAT3 non-kanonik, khususnya STAT3 mitokondria (mtSTAT3). Pada konteks ini, STAT3 tidak lagi berfungsi sebagai faktor transkripsi, melainkan sebagai regulator metabolisme dan respirasi mitokondria. Karena itu, dikembangkan pula mtSTAT3 inhibitors, yang secara spesifik menarget fungsi metabolik STAT3 tanpa secara langsung mengganggu transkripsi nuklear.
Jika semua pendekatan ini disatukan, ilustrasi tersebut menyampaikan satu kesimpulan besar: STAT3 bukan saklar on–off yang sederhana, melainkan simpul regulasi kompleks yang dapat dimodulasi dari berbagai arah. Inilah sebabnya strategi terapi modern tidak lagi bertanya “bagaimana cara mematikan STAT3?”, tetapi “di titik mana STAT3 sebaiknya dikendalikan agar manfaat maksimal dan efek samping minimal?”.
Dalam konteks pembelajaran, ilustrasi ini menegaskan bahwa pemahaman jalur sinyal bukan sekadar hafalan panah dan protein, melainkan dasar rasional untuk merancang strategi terapi berbasis mekanisme. STAT3 menjadi contoh ideal bagaimana satu protein dapat didekati melalui banyak pintu masuk terapeutik, sesuai dengan kebutuhan biologis dan klinis dari masing-masing penyakit (Samad et al., 2025).