- 5 Sections
- 8 Lessons
- Lifetime
- BAB I DARI SATU SEL KE KERAGAMAN PROSES BIOLOGIS (PERAN NUKLEUS DAN MATERI GENETIK)Bab ini menjadi fondasi konseptual masterclass dengan mengulas bagaimana seluruh keragaman sel dan proses biologis berawal dari satu sel tunggal, yaitu zigot. Pembahasan difokuskan pada peran sentral nukleus dan materi genetik dalam mengatur proliferasi, diferensiasi, serta spesialisasi sel. Mahasiswa diajak memahami bagaimana ekspresi gen, regulasi transkripsi, dan organisasi genom memungkinkan munculnya ratusan tipe sel dengan fungsi yang berbeda meskipun membawa informasi genetik yang sama. Bab ini menanamkan perspektif bahwa kompleksitas kehidupan bersumber dari regulasi, bukan sekadar keberadaan gen.2
- BAB II PROTEIN STAT3 SEBAGAI PENGAMBIL KEPUTUSAN MOLEKULER DALAM SEBUAH SELBab ini membahas STAT3 sebagai contoh konkret protein regulator yang berperan sebagai “decision maker” molekuler di dalam sel. STAT3 dipelajari tidak hanya sebagai faktor transkripsi, tetapi sebagai simpul integrasi berbagai sinyal ekstraseluler dan intraseluler. Pembahasan mencakup aktivasi STAT3, regulasi domain strukturalnya, serta implikasinya terhadap nasib sel, seperti proliferasi, diferensiasi, survival, dan respons stres. Bab ini menekankan bagaimana satu protein dapat menentukan arah perilaku sel melalui jaringan regulasi yang kompleks.4
- 2.12.1. Struktur dan Fungsi Protein STAT3 (Domain Protein, Target Inhibitor, dan Relevansinya pada Kondisi Normal dan Penyakit Osteoporosis)45 Minutes
- 2.2Kuis 2.14 Questions
- 2.32.2. Regulasi Aktivitas STAT3 oleh Jalur Persinyalan Hulu (Fokus JAK1/2–STAT3 Signaling, Senyawa Inhibitor JAK1/2, dan Implikasinya pada Rheumatoid Arthritis; RA)45 Minutes
- 2.4Kuis 2.24 Questions
- BAB III PENUAAN SEBAGAI PROSES BIOLOGIS YANG TERKONTROL DAN MENGARAH PADA DISREGULASIBab ini menggeser sudut pandang penuaan dari sekadar proses pasif akibat akumulasi kerusakan menjadi proses biologis yang relatif terprogram dan dikendalikan. Mahasiswa diajak memahami penuaan sebagai hasil perubahan bertahap dalam regulasi molekuler, jaringan sinyal, dan homeostasis seluler. Bab ini juga mengkaji bagaimana kegagalan mekanisme regulasi tersebut berujung pada kondisi disregulasi yang meningkatkan kerentanan terhadap penyakit degeneratif. Dengan demikian, penuaan diposisikan sebagai fenomena biologis yang dapat dipelajari, dimodelkan, dan berpotensi dimodulasi.4
- BAB IV INTERVENSI TERAPEUTIK MOLEKULER BERBASIS REGULASI SISTEMATIKBab ini membahas pendekatan terapeutik modern yang tidak lagi berfokus pada satu target tunggal, melainkan pada regulasi sistem biologis secara menyeluruh. Mahasiswa diperkenalkan pada konsep intervensi molekuler yang menargetkan jalur sinyal, jaringan regulasi gen, dan keseimbangan sistemik sel. Bab ini mengintegrasikan pengetahuan tentang STAT3, penuaan, dan regulasi sel untuk memahami bagaimana terapi dapat dirancang secara rasional, adaptif, dan kontekstual terhadap kompleksitas sistem biologis.4
- BAB V UJIAN AKHIR MASTERCLASS OSN #0001Bab ini merupakan tahap evaluasi akhir yang dirancang untuk mengukur pemahaman konseptual, kemampuan analisis, dan integrasi pengetahuan peserta terhadap seluruh materi masterclass. Ujian tidak hanya menilai penguasaan fakta, tetapi juga kemampuan berpikir tingkat tinggi, seperti penalaran biologis, interpretasi fenomena molekuler, dan penerapan konsep dalam konteks baru. Bab ini menegaskan tujuan utama masterclass, yaitu membentuk cara berpikir biologis yang sistemik, kritis, dan kompetitif sesuai standar OSN Biologi.3
Curriculum
2.1. Struktur dan Fungsi Protein STAT3 (Domain Protein, Target Inhibitor, dan Relevansinya pada Kondisi Normal dan Penyakit Osteoporosis)
2.1.1 STAT3 sebagai “pengambil keputusan” berbasis sinyal: dari membran ke inti sel
Jika di bab 1 (pelajaran 1.1 dan 1.2) kita menempatkan nukleus sebagai “ruang kendali”, maka pada bab 2 ini kita akan mulai mengenali salah satu “pejabat pengambil keputusan” yang sering muncul dalam berbagai konteks fisiologis dan patologis, yaitu protein Signal Transducer and Activator of Transcription 3 (STAT3). STAT3 merupakan protein yang sangat menarik karena STAT3 bekerja seperti “kurir” sekaligus “editor kebijakan”, yaitu menerima sinyal dari luar sel (misalnya sitokin dan faktor pertumbuhan/growth factor), kemudian menerjemahkannya menjadi keputusan transkripsi di dalam nukleus. Dalam banyak jalur persinyalan klasik, sinyal untuk STAT3 dimulai dari terbentuknya ikatan ligan-reseptor, yang kemudian akan mengaktifkan protein Janus kinases (JAK), lalu memfosforilasi STAT3. STAT3 yang telah difosforilasi pada asam amino tirosin nomor 705-nya akan memulai proses dimerisasi, bisa dengan sesama STAT3 (homodimer), namun bisa juga dengan protein lain, seperti STAT1. Komplek STAT3 dimer ini akan berpindah ke nukleus, dan selanjutnya mengatur ekspresi gen-gen targetnya. Narasi “membran → sitoplasma → nukleus → gen” ini adalah pola besar yang akan terus kia temui saat membahas inflamasi, kanker, penuaan, sampai penyakit tulang. Mekanisme umum aktivasi dan fungsi transkripsi STAT juga dibahas secara komprehensif pada literatur STAT klasik, termasuk bagaimana STAT3 memengaruhi fungsi sel melalui kontrol transkripsi (Samad et al., 2025) & Corry et al., 2014).
Pada konteks jaringan tulang, konsepnya menjadi sangat “hidup” karena tulang bukan struktur pasif. Tulang adalah organ dinamis yang terus mengalami remodeling tulang (bone remodeling). Remodeling tulang merupakan proses pemeliharaan tulang yang senantiasa mempertahankan keseimbangan antara proses pembentukan tulang yang dimediasi oleh osteoblas dan proses perombakan tulang yang dimediasi oleh osteoklas. Dalam konteks ini, osteoporosis dapat dipahami sebagai sebuah kondisi patologis yang terjadi pada seseorang bilamana keseimbangan semacam ini bergeser. Pada pasien osteoporosis, resorpsi tulang cenderung lebih dominan daripada formasi tulang baru. Corry dkk., (2014) menjelaskan kerangka besar ini sekaligus menempatkan STAT3 sebagai salah satu simpul penting yang terhubung dengan sinyal sitokin (terutama keluarga IL-6/gp130) pada sel-sel tulang.
2.1.2 Peta lengkap domain STAT3: mengapa struktur menentukan fungsi
Agar tidak sekadar “menghafal jalur”, kita perlu melihat STAT3 sebagai sebuah protein modular. Setiap bagian (domain) pada protein STAT3 merupakan komponen fungsional yang dapat menjadi titik kontrol untuk aktivitas tertentu. Oleh karena itu, domain-domain pada protein STAT3 juga dijadikan sebagai target dari aktivitas penghambatan (inhibition) atau pengaktivan (activation). Menurut Samad et al. (2025), secara arsitektur, STAT3 terdiri dari beberapa domain utama yang bekerja berurutan sebagai satu rangkaian fungsi, yaitu:
- Domain ujung amino (N-terminal domain; NTD) pada protein STAT3 berperan dalam pengaturan interaksi antarmolekul STAT3, baik dengan sesama STAT3 maupun dengan protein regulator lainnya. Selain itu, NTD berkontribusi penting dalam menjaga stabilitas kompleks STAT3, khususnya pada tahap awal pembentukan dan pemeliharaan aktivitas transkripsi.
- Domain koil-koil (coiled-coil domain; CCD) berfungsi sebagai platform interaksi protein–protein bagi berbagai protein pengatur STAT3, termasuk ko-aktivator dan ko-represor transkripsi, protein adaptor sinyal, serta regulator negatif STAT3 (misalnya SOCS dan PIAS, secara tidak langsung). Dengan demikian, CCD berperan menentukan protein mana yang dapat berinteraksi dengan STAT3 selama siklus aktivasi dan inaktivasi, sehingga memengaruhi konteks dan keluaran biologis sinyal STAT3.
- Domain pengikat DNA (DNA-binding domain; DBD) merupakan domain yang menentukan kemampuan STAT3 untuk mengenali dan berikatan dengan sekuens DNA target, khususnya pada wilayah promotor gen-gen targetnya. Interaksi spesifik antara DBD dan DNA ini menjadi prasyarat utama bagi STAT3 untuk menjalankan fungsinya sebagai faktor transkripsi.
- Domain penghubung (linker domain) berperan dalam mengatur orientasi spasial dan koordinasi fungsional antara domain pengikat DNA dan domain SH2. Domain ini turut memengaruhi sensitivitas STAT3 terhadap senyawa inhibitor, khususnya yang menargetkan domain SH2. Selain itu, linker domain memiliki potensi sebagai target alternatif terapi berbasis inhibitor alosterik, yaitu senyawa yang tidak mengganggu proses fosforilasi STAT3, tetapi secara spesifik menghambat fungsi transkripsinya.
- Domain SH2 (Src homology 2 domain) pada protein STAT3 berperan krusial dalam proses dimerisasi STAT3. Aktivitas domain ini bergantung pada status fosforilasi residu tirosin nomor 705 (Tyr705). STAT3 akan memulai proses dimerisasi ketika Tyr705 difosforilasi menjadi fosfotirosin, sehingga memungkinkan dua molekul STAT3 berpasangan dan selanjutnya berpindah ke nukleus.
- Domain transaktivasi (transactivation domain; TAD) yang terletak di ujung karboksil (C-terminal) protein STAT3 berfungsi sebagai “tombol gas” transkripsi, yaitu dengan merekrut ko-aktivator serta komponen mesin transkripsi. Melalui domain ini, STAT3 secara langsung mengaktifkan ekspresi gen-gen target yang terlibat dalam berbagai proses biologis.
2.1.3 Klasifikasi inhibitor STAT3 berbasis domain target (dengan contoh senyawanya)
Pada pelajaran ini, pengetahuan mengenai senyawa penghambat (inhibitor) STAT3 disusun berdasarkan logika struktur domain protein. Pendekatan ini bertujuan agar mahasiswa tidak sekadar “mengoleksi nama obat”, melainkan memahami alasan molekuler mengapa suatu inhibitor dapat bekerja, domain apa yang ditargetkan, dan konsekuensi biologis dari penghambatan tersebut.
a) Inhibitor yang menargetkan domain SH2 (paling banyak dikaji)
Domain SH2 merupakan target yang paling sering dibahas karena perannya yang sangat krusial dalam pengenala
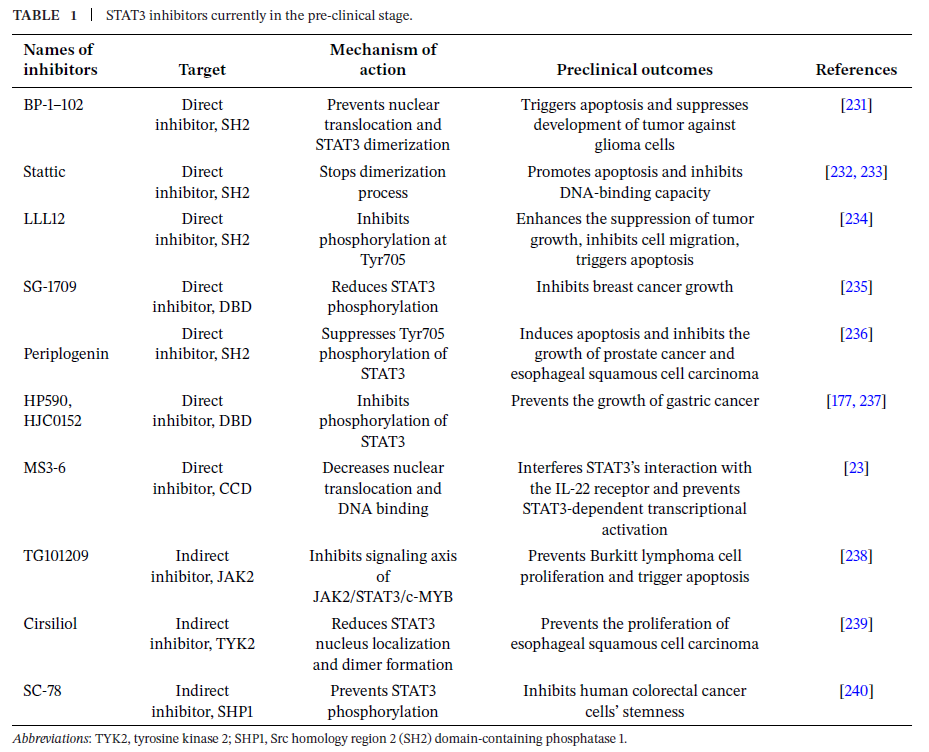
n residu fosfotirosin dan pembentukan dimer STAT3. Dimerisasi ini merupakan langkah penentu sebelum STAT3 dapat berpindah ke nukleus dan mengaktifkan transkripsi gen target. Oleh karena itu, penghambatan domain SH2 secara langsung mengganggu aktivasi STAT3 pada tingkat yang sangat fundamental.
Dalam tinjauan komprehensif oleh MedComm (2025), inhibitor domain SH2 diklasifikasikan sebagai kelompok besar yang mencakup senyawa molekul kecil (small molecules) serta pendekatan lain yang bertujuan menghambat proses dimerisasi dan aktivasi STAT3. Beberapa inhibitor yang sering digunakan sebagai contoh representatif dalam diskusi akademik antara lain Stattic, S3I-201, STA-21, dan BP-1-102, bersama dengan berbagai kandidat lain yang dirangkum dalam literatur tersebut (Lim & Cao, 2006; Samad et al., 2025).
Makna biologisnya, penghambatan domain SH2 umumnya menyebabkan penurunan ekspresi gen target STAT3 karena STAT3 gagal membentuk dimer yang kompeten untuk menjalankan fungsi transkripsionalnya.
b) Inhibitor yang menargetkan domain pengikat DNA (DNA-binding domain; DBD)
Kelompok inhibitor ini menarget kemampuan STAT3 untuk berikatan langsung dengan DNA, khususnya pada elemen respons di wilayah promotor gen target. Pendekatan ini tidak selalu menghambat aktivasi atau translokasi STAT3 ke nukleus, tetapi secara spesifik menghalangi langkah eksekusi transkripsi.
Dalam tinjauan yang sama, inhibitor berbasis DBD mencakup senyawa molekul kecil maupun strategi berbasis asam nukleat, seperti oligonukleotida decoy STAT3 (STAT3 decoy ODN). Strategi decoy bekerja dengan menyediakan “umpan” DNA sintetis sehingga STAT3 berikatan dengan sekuens palsu tersebut, bukan dengan promotor gen targetnya (Samad et al., 2025).
Makna biologisnya, meskipun STAT3 berhasil teraktivasi dan masuk ke nukleus, ia tidak mampu menjalankan fungsi transkripsional secara efektif apabila tidak dapat berikatan dengan elemen DNA target.
c) Inhibitor yang menargetkan domain koil-koil (coiled-coil domain; CCD)
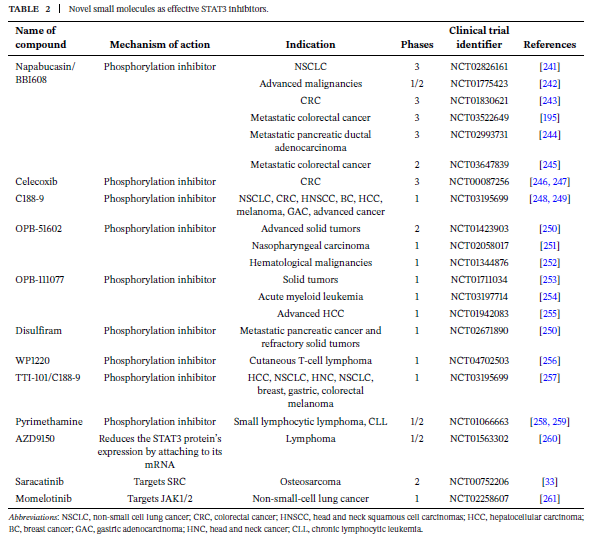
Domain koil-koil berperan penting dalam interaksi protein–protein serta dalam pengorganisasian kompleks transkripsi STAT3. Penghambatan domain ini tidak secara langsung mematikan fosforilasi atau dimerisasi, tetapi mengganggu perakitan dan stabilitas kompleks protein yang diperlukan agar STAT3 bekerja secara optimal.
Tinjauan MedComm (2025) juga melaporkan adanya pendekatan inhibitor yang diarahkan ke domain ini, dengan MS3-6 sebagai salah satu contoh senyawa yang merepresentasikan strategi penargetan CCD.
Makna biologisnya, pendekatan ini dapat dipahami sebagai upaya untuk mengganggu komunikasi dan koordinasi antarkomponen molekuler, sehingga aktivitas STAT3 menjadi kurang stabil dan kurang selektif dalam mengatur ekspresi gen.
d) Inhibitor yang menargetkan ekspresi protein STAT3 dan pendekatan berbasis penghancuran protein (protein degradation)
Selain menghambat fungsi domain tertentu, terdapat strategi yang lebih hulu, yaitu menurunkan jumlah protein STAT3 itu sendiri. Dalam tinjauan MedComm (2025), pendekatan ini diwakili antara lain oleh STAT3 antisense oligonucleotide (ASO), yang bekerja dengan menekan ekspresi STAT3 pada tingkat mRNA.
Di sisi lain, pendekatan modern yang semakin berkembang adalah targeted protein degradation, misalnya melalui teknologi PROTAC. Strategi ini tidak sekadar menghambat satu domain fungsional, melainkan secara aktif mengarahkan STAT3 untuk didegradasi oleh sistem proteasom seluler (Bromberg & Darnell, 2000).
Makna biologisnya, pendekatan ini mengubah paradigma dari sekadar inhibisi aktivitas menjadi pengurangan stok protein STAT3. Pada konteks tertentu, strategi ini dapat lebih efektif, namun juga menuntut tingkat selektivitas yang sangat tinggi agar tidak mengganggu fungsi fisiologis STAT3 yang masih diperlukan oleh sel.
2.1.4 Mengapa STAT3 relevan untuk osteoporosis: dua sisi tulang (osteoklas dan osteoblas)
Relevansi STAT3 dalam konteks osteoporosis menjadi semakin jelas ketika proses remodeling tulang dipahami sebagai hasil keseimbangan dinamis antara dua jenis sel utama, yaitu osteoklas sebagai sel peresorpsi tulang dan osteoblas sebagai sel pembentuk tulang. Ilustrasi yang disusun oleh Washil Insan Karim menggunakan BioRender secara visual merangkum posisi strategis STAT3 sebagai simpul molekuler yang menghubungkan sinyal ekstraseluler dengan keputusan transkripsi di dalam nukleus, baik pada jalur osteoklastogenesis maupun osteoblastogenesis.
Pada sisi osteoklas, ilustrasi tersebut menunjukkan bahwa aktivasi STAT3 dimulai dari berbagai sinyal sitokin, terutama IL-6 yang berikatan dengan kompleks reseptor gp130, serta sinyal lain seperti LIF dan leptin. Aktivasi reseptor ini memicu fosforilasi JAK2, yang selanjutnya memfosforilasi STAT3 pada residu Tyr705. STAT3 terfosforilasi kemudian mengalami dimerisasi, berpindah ke nukleus, dan mengaktifkan transkripsi gen-gen target. Dalam konteks osteoklas, salah satu target kunci jalur ini adalah NFATc1, regulator utama diferensiasi osteoklas. Jalur ini divisualisasikan pada ilustrasi sebagai
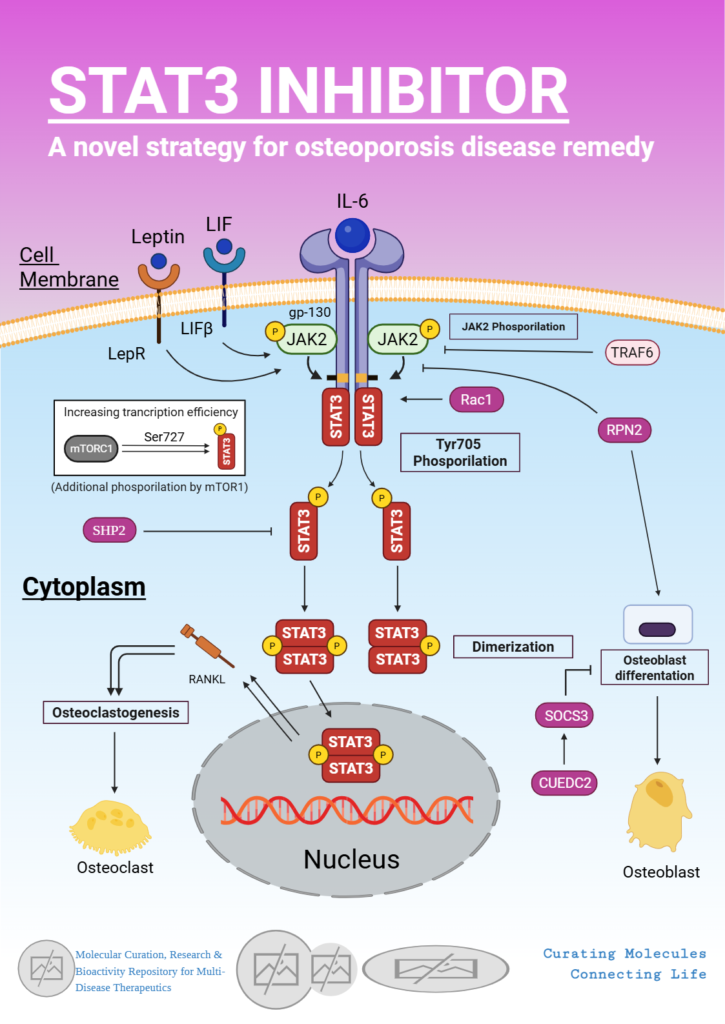
alur yang berujung pada peningkatan osteoklastogenesis dan aktivitas resorpsi tulang.
Temuan eksperimental oleh Yang dkk. (2019) memberikan landasan kuat bagi narasi ini. Studi tersebut menunjukkan bahwa penghapusan Stat3 secara spesifik pada osteoklas meningkatkan massa tulang, terutama karena diferensiasi dan fungsi osteoklas mengalami penurunan. Mekanisme molekulernya melibatkan berkurangnya aktivasi transkripsi NFATc1 akibat hilangnya aktivitas STAT3. Ilustrasi mahasiswa ini selaras dengan temuan tersebut, karena secara eksplisit menempatkan STAT3 sebagai penghubung antara sinyal sitokin dan ekspresi gen pro-osteoklastogenik. Selain itu, ilustrasi juga menampilkan penghambatan STAT3 oleh senyawa seperti Stattic, yang mengganggu fungsi domain SH2 dan dimerisasi STAT3, sehingga menurunkan sinyal menuju nukleus dan berpotensi menekan osteoklastogenesis.
Pada sisi osteoblas, ilustrasi yang sama menegaskan bahwa STAT3 tidak semata-mata berperan sebagai promotor resorpsi tulang. Jalur STAT3 juga terlibat dalam program diferensiasi osteoblas, yang divisualisasikan sebagai jalur paralel menuju pembentukan tulang. Sinyal STAT3 pada osteoblas berinteraksi dengan regulator homeostasis tulang, termasuk mekanisme umpan balik negatif melalui SOCS3 dan protein pengatur lain seperti CUEDC2, yang ditampilkan pada ilustrasi sebagai pengendali intensitas sinyal.
Peran ganda STAT3 pada osteoblas diperkuat oleh studi Zhou dkk. (2021), yang menunjukkan bahwa delesi Stat3 pada osteoblas menyebabkan gangguan perkembangan skeletal, osteoporosis, dan peningkatan risiko fraktur. Temuan ini menegaskan bahwa STAT3 diperlukan untuk mempertahankan fungsi osteoblas dan homeostasis tulang normal. Dengan demikian, ilustrasi tersebut membantu memperjelas bahwa STAT3 bukan sekadar “penggerak osteoklas”, melainkan regulator konteks-spesifik yang dapat memberikan efek protektif atau merugikan tergantung pada jenis sel dan kondisi fisiologisnya.
Tinjauan sistemik oleh Li dkk. (2022) merangkum kompleksitas ini dengan menempatkan STAT3 sebagai simpul utama pada poros RANKL–STAT3–NFATc1 di sisi osteoklas, serta sebagai bagian dari jejaring regulasi osteogenesis di sisi osteoblas, termasuk interaksinya dengan faktor-faktor diferensiasi osteoblas seperti Runx2 dan marker osteogenesis lainnya. Ilustrasi BioRender yang disusun mahasiswa secara efektif menerjemahkan kerangka konseptual ini ke dalam representasi visual yang mudah diikuti, memperlihatkan bagaimana satu protein yang sama dapat berada di pusat dua proses biologis yang saling berlawanan.
Daftar Referensi:
- Samad, M. A., Ahmad, I., Hasan, A., Alhashmi, M. H., Ayub, A., Al-Abbasi, F. A., Kumer, A., & Tabrez, S. (2025). STAT3 Signaling Pathway in Health and Disease. MedComm, 6(4), e70152. https://doi.org/10.1002/mco2.70152
- Bromberg, J., & Darnell, J. E., Jr. (2000). The role of STATs in transcriptional control and their impact on cellular function. Oncogene, 19(21), 2468–2473.
- Corry, K. A., Zhang, P., & Li, J. (2014). Stat3 Signaling Cascade in the Differentiation, Growth and Functions of Bone Cells. Orthopedic & Muscular System: Current Research (Special Issue), S2:008.
- Levy, D. E., & Darnell, J. E., Jr. (2002). Stats: transcriptional control and biological impact. Nature Reviews Molecular Cell Biology, 3(9), 651–662.
- Li, J., Yin, Z., Huang, B., Xu, K., & Su, J. (2022). Stat3 Signaling Pathway: A Future Therapeutic Target for Bone-Related Diseases. Frontiers in Pharmacology, 13, 897539.
- Lim, C. P., & Cao, X. (2006). Structure, function, and regulation of STAT proteins. Molecular BioSystems, 2(11), 536–550.
- Sanpaolo, E. R., Rotondo, C., Cici, D., Corrado, A., & Cantatore, F. P. (2020). JAK/STAT pathway and molecular mechanism in bone remodeling. Molecular Biology Reports, 47(11), 9087–9096.
- Yang, Y., Chung, M. R., Zhou, S., et al. (2019). STAT3 controls osteoclast differentiation and bone homeostasis by regulating NFATc1 transcription. Journal of Biological Chemistry, 294(42), 15395–15407.
- Zhou, S., Dai, Q., Huang, X., et al. (2021). STAT3 is critical for skeletal development and bone homeostasis by regulating osteogenesis. Nature Communications, 12, 6891.